Medikamente für Frauen nach der Menopause
- Autor(en): Etzel Gysling
- pharma-kritik-Jahrgang 38
, Nummer 3, PK992
Redaktionsschluss: 9. Juni 2016
DOI: https://doi.org/10.37667/pk.2016.992 - PDF-Download der Printversion dieser pharma-kritik Nummer
Vierzehn Jahre, nachdem die wichtigsten Studienresultate der «Women’s Health Initiative» (WHI) veröffentlicht worden sind, wird die Verabreichung von weiblichen Sexualhormonen in oder nach der Menopause immer noch sehr unterschiedlich beurteilt. In der Zwischenzeit sind einige kleinere Studien sowie eine Reihe von Leitlinien publiziert worden. Im vorliegenden Text wird der aktuelle Wissensstand zusammengefasst und zu praxisrelevanten Fragen Stellung genommen. Auf eine detaillierte Schilderung der klimakterischen Symptome wird hier verzichtet.
Die Medikamente
Die verfügbaren hormonalen und nicht-hormonalen Medikamente haben ein unterschiedliches Nutzen/Risiko-Profil; ihre erwünschten und unerwünschten Wirkungen sind jedoch keineswegs einheitlich gut dokumentiert. Die folgende Übersicht orientiert zunächst über die Erhältlichkeit und Zulassung der verschiedenen Medikamente; zu den meisten dieser Substanzen finden sich weiter differenzierte Informationen in den Abschnitten «Probleme der Hormone» und «Indikationen».
Östrogene
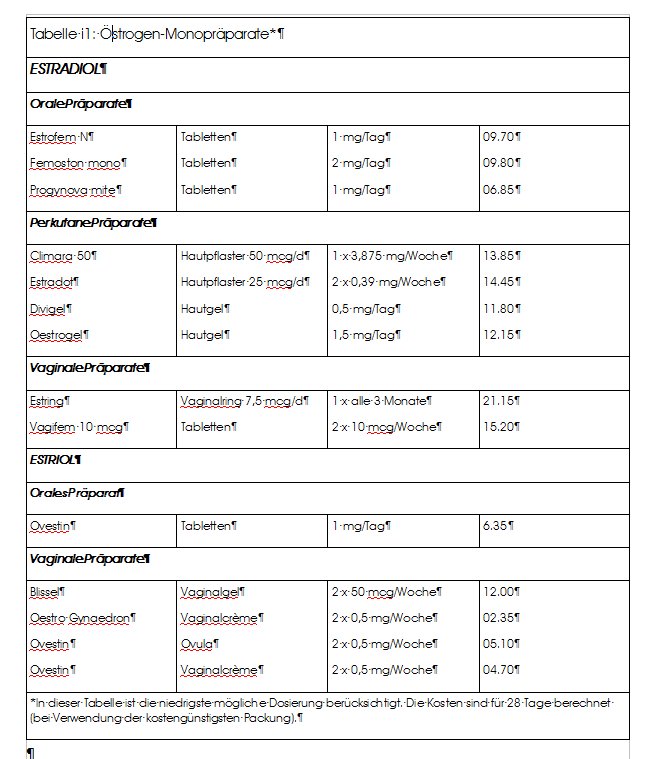
In den WHI-Studien wurde das traditionelle, aus Stutenharn gewonnene Präparat mit konjugierten Östrogenen (zusammen mit Medroxyprogesteron: Premarin®, heute in der Schweiz nicht mehr erhältlich) verwendet. Aktuell empfehlen die Fachgesellschaften, als oral anwendbares Östrogen Estradiol (Estrofem® u.a.) einzusetzen. Estradiol-Monopräparate sind auch zwei Hautpflaster (Climara® und Estradot®) sowie zwei Gels zur kutanen Applikation (Divigel®, Oestrogel®). Wegen der Gefahr eines Endometriumkarzinoms ist Estradiol als Monotherapie jedoch nur bei Frauen zu empfehlen, die hysterektomiert sind. Ausserdem sind zwei Estradiol-haltige Präparate zur vaginalen Anwendung erhältlich (siehe Tabelle i1). Gelegentlich gelangt auch noch der (weniger aktive) Estradiol-Metabolit Estriol zum Einsatz (überwiegend zur vaginalen Anwendung, Tabelle i1).
Gestagene
Gestagene werden in und nach der Menopause meistens in fixen Kombinationspräparaten (mit Östrogen zusammen) verordnet. Medroxyprogesteron, das in der WHI-Studie bei Frauen mit intaktem Uterus gegeben wurde, steht jedoch auch separat zur Verfügung (Depot-Provera®, Prodafem®). Auch andere Gestagene (Dyrogesteron, Progesteron) sind als Monopräparate erhältlich, siehe Tabelle i2. In einem Intrauterin-System ist Levonorgestrel enthalten (Mirena®, LNG-IUS), das zum langfristigen Endometrium-Schutz eingesetzt werden kann.
Östrogen-Gestagen-Kombinationspräparate
Bei Frauen mit intaktem Uterus kommen – sofern eine hormonale Therapie indiziert ist – in erster Linie kombinierte Östrogen-Gestagen-Präparate in Frage. Wie die Tabelle 1 zeigt, sind Kombinationen von Estradiol mit verschiedenen Gestagenen erhältlich. Teilweise kommt eine ständig identische Tagesdosis der beiden Hormone zur Anwendung («Einphasenpräparate»); oft enthalten die Präparate primär nur das Östrogen und erst in einer zweiten Phase auch ein Gestagen («sequentielle» Therapie). Neben den oralen Präparaten sind auch Hautpflaster von Estradiol/Norethisteron erhältlich, siehe Tabelle 1 (Seite 12).
Androgene
Da in der Menopause auch die Androgenspiegel abnehmen, empfehlen die Fachgesellschaften bei sexuellen Störungen unter anderem einen Behandlungsversuch mit Testosteron. In der Schweiz existiert kein Testosteron-Präparat mit einer entsprechenden Zulassung.
Weitere Hormonpräparate
Tibolon (Livial® u.a.), ein synthetisches Steroidhormon mit östrogenen, gestagenen und androgenen Eigenschaften, ist zur Symptomtherapie nach der Menopause zugelassen (mindestens 12 Monate nach der letzten natürlichen Regelblutung). Da das Risikoprofil von Tibolon (Livial® u.a.) nicht nennenswert von demjenigen einer kombinierten Östrogen-Gestagen-Therapie abweicht, wird Tibolon im Folgenden nicht mehr separat erwähnt.
Eine Kombination von konjugierten Östrogenen (aus Stutenharn) und Bazedoxifen, einem «selective estrogen receptor modulator» (SERM) ist unter dem Namen Duavive® in der Schweiz zugelassen, aber aktuell (Juni 2016) nicht im Handel. Ospemifen (Osphena®) ist ein weiterer SERM, der in den USA zur Behandlung von Atrophie-Symptomen im Genitalbereich zugelassen ist.
Vor- oder Nachteile der vor allem in den USA unter der Bezeichnung «compounded bioidentical hormones» propagierten Präparate sind nicht genügend dokumentiert.(1)
Nicht-hormonale Medikamente
In den Leitlinien der verschiedenen Fachgesellschaften werden verschiedene nicht-hormonale Symptomtherapien erwähnt, die mindestens teilweise in klinischen Studien geprüft worden sind.
Extrakte aus der Wurzel der Traubensilberkerze (Cimicifuga racemosa, verschiedene Präparate) sind offiziell zur Behandlung von menopausalen Beschwerden zugelassen und limitiert kassenzulässig. Die aktuell vorliegenden Daten genügen jedoch nicht, um eine Wirksamkeit dieser Präparate als erwiesen anzusehen.(2) Dasselbe gilt für Kombinationen von Cimicifuga- und Johanniskraut-Extrakten. In der Schweiz ist ferner ein Extrakt von Salbeiblättern (Menomed®) für dieselbe Indikation zugelassen, aber nicht genügend dokumentiert (und auch nicht kassenzulässig).
Ausserdem werden in den Leitlinien verschiedene psychotrope oder neurotrope Medikamente zur Behandlung der vasomotorischen Symptome («Wallungen») empfohlen. Es handelt sich um Substanzen, die bei dieser Indikation in der Regel gegen Placebo geprüft wurden, jedoch ausnahmslos nicht über eine entsprechende offizielle Zulassung verfügen. Zu nennen sind der Alpha-Agonist Clonidin (Catapresan®), das Antiepileptikum Gabapentin (Neurontin® u.a.), verschiedene selektive Serotonin-Wiederaufnahmehemmer (SSRI: Citalopram, Fluoxetin, Paroxetin) sowie der Noradrenalin-Serotonin-Wiederauf-nahmehemmer Venlafaxin (Efexor® u.a.).
Probleme der Hormone
Kardiovaskuläre Ereignisse
Gemäss den Resultaten der WHI-Studien treten unter der kombinierten (oralen) Östrogen-Gestagen-Therapie vermehrt Herzinfarkte, Schlaganfälle und thromboembolische Ereignisse auf.
Eine aktuelle Cochrane-Analyse bestätigt das erhöhte kardiovaskuläre Risiko unter der Hormontherapie. So muss mit einem zusätzlichen Schlaganfall gerechnet werden, wenn 165 Frauen hormonal behandelt werden. Das erhöhte Schlaganfall-Risiko manifestiert sich nach zwei Jahren kombinierter Östrogen-Gestagen-Therapie bzw. nach vier Jahren Östrogen-Monotherapie.(3) In einer Subgruppenanalyse wurde die Rolle des zeitlichen Abstands von der Menopause untersucht: nur bei Frauen, die schon früh (weniger als 10 Jahre) nach der Menopause eine Hormontherapie erhalten, kann kein sicherer Einfluss auf das Schlaganfall-Risiko festgestellt werden.(3)
Auch venöse Thrombosen und Lungenembolien sind unter Hormontherapie gesamthaft signifikant häufiger als bei Frauen, die keine Hormone erhalten. Am höchsten ist dieses Risiko im ersten Jahr der Behandlung. Unter einer kombinierten Hormontherapie sind thromboembolische Ereignisse eindeutig häufiger zu beobachten als unter Östrogenen allein, wobei dieser Unterschied bei einer längerdauernden Behandlung deutlicher wird. Bei älteren und übergewichtigen Frauen besteht ein noch höheres Thromboembolie-Risiko.(3)
Dagegen findet sich nach der Cochrane-Analyse keine Evidenz, dass Herzinfarkte unter Hormontherapie gesamthaft häufiger auftreten oder dass die Gesamtmortalität erhöht wäre. Wird die Hormontherapie früh (weniger als 10 Jahre) nach der Menopause begonnen, errechnet sich bezüglich koronarer Erkrankungen und Mortalität ein Vorteil für die hormonbehandelten Frauen. Bei Frauen, die erst spät (10 oder mehr Jahre nach der Menopause) mit der Hormontherapie beginnen, lässt sich kein sicherer Einfluss auf das koronare Risiko oder die Mortalität feststellen.(3)
Zusammenfassend kommt die Cochrane-Analyse zum Schluss, eine Hormontherapie bringe Frauen nach der Menopause keinen oder nur einen minimalen kardiovaskulären Nutzen und erhöhe das Schlaganfall- und Thromboembolie-Risiko. Daran ändern auch neuere Publikationen nichts, die einen Nutzen der Hormontherapie propagieren(4) – das Design der entsprechenden Studien erlaubt keine sicheren Schlüsse.
Ergänzende Untersuchungen lassen vermuten, dass Estradiol (oral oder transdermal verabreicht) ein geringeres kardiovaskuläres Risiko beinhaltet als die konjugierten Östrogene;(5,6) entsprechende randomisierte Studien liegen aber bisher nicht vor. Auch die Annahme, transdermal applizierte Hormone hätten allgemein ein kleineres kardiovaskuläres Risiko als oral verabreichte,(7) beruht ausschliesslich auf nicht-randomisierten Studien. Nach dem Absetzen der Hormone kann jedoch mit dem allmählichen Verschwinden des erhöhten vaskulären Risikos gerechnet werden.
Brustkrebs
Eine kombinierte Östrogen-Gestagen-Therapie erhöht das Risiko, an einem Brustkrebs zu erkranken.(8) Das kumulative Risiko ist um etwa 25% höher als ohne Hormone. Wird diese Behandlung für 8 Jahre fortgesetzt, so werden bei 1000 behandelten Frauen im Vergleich mit der unbehandelten Kontrollgruppe 7 zusätzliche Brustkrebs-Fälle manifest. Auch die Brustkrebs-Mortalität ist erhöht.(9) Am höchsten ist das Risiko offenbar für Frauen, die früh (kurz nach dem Einsetzen der Menopause) behandelt werden.(10) Es ist nicht klar, ob verschiedene Gestagene oder der Verabreichungsmodus (oral oder transdermal) das Risiko in unterschiedlicher Weise beeinflussen.(11) Selbst nach dem Absetzen der Hormone kann das Brustkrebs-Risiko noch erhöht bleiben.(12)
Bei Frauen mit einer Brustkrebs-Anamnese erhöht die Hormontherapie das Risiko eines Rückfalls signifikant.(13,14)
Nur mit Östrogenen behandelte Frauen erkranken dagegen seltener an einem Brustkrebs, ein Unterschied, der allerdings erst nach annähernd 11 Jahren statistische Signifikanz erlangt.(15)
Ovarialkarzinom
Unter einer Hormontherapie sind Ovarialkarzinome häufiger als ohne Hormone. Eine von 1000 Frauen, die fünf Jahre lang Hormone erhalten, erkrankt an einem Ovarialkarzinom.(16) Wahrscheinlich spielt es keine Rolle, ob nur Östrogene oder auch Gestagene verwendet werden. Es ist auch nicht bekannt, ob der Verabreichungsmodus (oral oder transdermal) bedeutsam ist. Nach dem Absetzen der Therapie nimmt das Risiko allmählich wieder ab.
Erkrankungen der Gallenwege
Gallensteine und entsprechend auch Cholezystitiden und Cholezystektomien werden unter einer Hormontherapie gehäuft beobachtet. In einer prospektiven Kohortenstudie waren davon nur Frauen betroffen, die ein orales Östrogen-Monopräparat erhielten,(17) in einer weiteren Kohortenstudie hatten aber auch Frauen Gallenblasen-Probleme, die eine kombinierte Therapie erhielten.(18) Auch in der letzteren Studie waren Gallensteine aber unter oralen Präparaten häufiger als unter transdermalen. Nach dem Absetzen der Hormone nimmt das erhöhte Risiko über einige Jahre allmählich ab.
Weitere Probleme
Mit Hormonen behandelte Frauen haben häufiger Nierensteine: in den WHI-Studien wurden auf 10'000 Frauenjahre 39 Fälle von Nephrolithiasis beobachtet, 5 mehr als unter Placebo. Dies war unabhängig davon, ob auch Gestagene verabreicht wurden. Frauen, die auch Calcium/Vitamin D-Präparate nahmen, waren jedoch besonders häufig betroffen. (Auch in der separaten WHI-Studie, in der die Wirkung von Calcium- und Vitamin-D-Supplementen untersucht wurde, traten unter den Supplementen 17% mehr Nierensteine auf.(19))
Ebenfalls in den WHI-Studien trat bei Frauen, die zu Studienbeginn keine Harninkontinenz hatten, dieses Problem unter der Hormontherapie signifikant häufiger auf als unter Placebo.
Bei älteren Frauen (über 65) waren in den WHI-Studien auch kognitive Probleme (mässige kognitive Beeinträchtigung, aber auch Demenzen) häufiger, wenn die Frauen Hormone erhielten.
Indikationen
In den letzten Jahren haben sich also keine neuen Erkenntnisse ergeben, wonach vom Prinzip abgewichen werden sollte, Frauen nach der Menopause keine langfristige «präventive» Hormontherapie zu offerieren. Ein Teil der Frauen hat aber in und kurz nach der Menopause unangenehme Symptome, die einer Behandlung bedürfen.
Vasomotorische Symptome
Vasomotorische Symptome (Hitzewallungen, nächtliche Schweissausbrüche) sind quasi das dominierende Problem der Menopause. Eine Minderheit von Frauen hat so starke Beschwerden, dass sich eine Therapie aufdrängt. Die «Hormonsubstitution» ist in diesen Fällen zweifellos die wirksamste Therapie. Dabei soll nach dem Grundsatz behandelt werden, die Hormone so kurzfristig und so niedrig dosiert wie möglich zu verabreichen. Die Intervention ist aber auch so nicht risikofrei: Wie oben beschrieben, sind thromboembolische Ereignisse im ersten Behandlungsjahr am häufigsten und die kombinierte Östrogen-Gestagen-Therapie erhöht das Brustkrebs-Risiko kurz nach der Menopause am stärksten. Deshalb sollen sich die betroffenen Frauen nach ausführlicher Besprechung am therapeutischen Entscheid mitbeteiligen.
Bei der Wahl eines kombinierten Östrogen-Gestagen-Präparates (für Frauen mit intaktem Uterus) steht die Estradiol/Norethisteron-Kombination im Vordergrund. Diese ist sowohl in oralen Formen (Ein- und Mehrphasenpräparate) als auch zur transdermalen Applikation als Hautpflaster verfügbar und kann deshalb gut individualisiert werden. Ob aber Hautpflaster tatsächlich eine günstigere Nutzen/Risiko-Bilanz aufweisen als orale Präparate, ist nicht genügend gesichert. Eine Substitution mit separaten Östrogen- und Gestagen-Präparaten hat in der Regel keine nennenswerten Vorteile. Auch die Kombination von Estradiol mit dem Levonorgestrel-Intrauterinsystem ist für eine Therapie, die möglichst bald wieder abgebaut werden soll, wenig sinnvoll. Da die verschiedenen Gestagene praktisch nicht in Studien mit klinischen Endpunkten verglichen worden sind, kann anderen Gestagenen gegenüber Norethisteron keine Überlegenheit zugeschrieben werden. Sie sind teilweise von ungünstigen Studienresultaten (Medroxyprogesteron in den WHI-Studien) bzw. von einem möglicherweise höheren Thromboembolie-Risiko (Cyproteron, Drospirenon) belastet. Ähnliche Überlegungen gelten für Tibolon.
Für Frauen, bei denen der Uterus entfernt worden ist, gelangt ein Estradiol-Monopräparat zum Einsatz – eine Therapie, die gesamthaft weniger Risiken aufweist als diejenige mit den Hormonkombinationen. Gegen eine langfristige Verabreichung spricht jedoch auch hier, dass die Therapie keineswegs risikofrei ist (siehe oben). Es stehen orale Präparate und Hautpflaster zur Verfügung.
Wenn die vasomotorischen Symptome nicht mit einer Hormontherapie behandelt werden sollen, werden in den aktuellen Leitlinien die oben kurz beschriebenen Alternativen (Cimicifuga usw.) empfohlen. Obwohl es für einzelne dieser Mittel eine entsprechende Zulassung oder einige wenige klinische Studienresultate gibt, verfügt keine dieser medikamentösen Optionen über eine überzeugende Nutzen/Risiko-Bilanz. Cimicifuga wirkt zu wenig zuverlässig und andere Mittel wie z.B. die SSRI bringen ein zu hohes Nebenwirkungspotential mit sich.
Die Wirkung von nicht-medikamentösen Interventionen ist zwar im Ganzen auch nicht zuverlässig gesichert. Diese haben jedoch den Vorteil, keine problematischen Nebenwirkungen zu verursachen. Mit der Nahrung zugeführte «Phytoöstrogene» (Isoflavone in Hülsenfrüchten, Lignane in Lein- und Sesamsamen) können möglicherweise die Intensität der Symptome mindern.(20) Zur Akupunktur liegen widersprüchliche Daten vor; gemäss einer Meta-Analyse ist ein günstiger Effekt auf die Häufigkeit und Intensität vasomotorischer Symptome wahrscheinlich.(21) Körperliches Training («Fitness») beeinflusst die vasomotorischen Symptome kaum, kann jedoch das allgemeine Wohlbefinden verbessern. Auch eine kognitive Verhaltenstherapie kann sich offenbar gut auswirken.(22)
Uro-genitales Syndrom
In und besonders nach der Menopause sind auch Beschwerden im Bereich der Urogenitalorgane häufig. Unter den Begriff des «genito-urinary syndrome of menopause» fallen ganz verschiedene Symptome: Trockenheit, Irritation/Brennen und Atrophie im Bereich der genitalen Schleimhäute, Dyspareunie, übermässiger Harndrang, allenfalls auch Harninkontinenz. Diese Symptome sollen sich gemäss der allgemein akzeptierten Meinung in erster Linie durch die lokale (vaginale) Applikation von niedrigen Östrogen-Dosen bessern lassen. In der Schweiz stehen verschiedene Estradiol- und Estriol-Präparate zur vaginalen Therapie zur Verfügung, z.B. Estring®, ein Vaginalring, Vagifem®-Tabletten, Ovestin®-Ovula und -Crème (siehe auch Tabelle i1). Auch in dieser Weise verabreichte Hormone werden systemisch verfügbar; eine regelmässige, langfristige Therapie ist deshalb nicht völlig risikofrei, insbesondere auch nicht hinsichtlich eines Endometriumkarzinoms. Eine befeuchtende hormonfreie Lokalbehandlung (z.B. mit einem Gel auf Wasserbasis) ist deshalb in vielen Fällen die Option, die primär berücksichtigt werden sollte.
Psychische Symptome
Unter den «klimakterischen» Beschwerden werden oft auch psychische Symptome wie Schlafstörungen und eine Tendenz zu Verstimmung und Depressionen genannt. Unmittelbar vor und in der Menopause sind Frauen, die schon früher depressive Episoden hatten, am ehesten Depressions-gefährdet. Nach der Menopause nimmt die Häufigkeit von Depressionen ab.
Die Zusammenhänge zwischen der hormonalen Umstellung und psychischen Symptomen sind jedoch nicht klar. Dass sich vasomotorische Symptome mit gestörter Nachtruhe auf die Psyche auswirken können, ist einleuchtend. Entsprechend gibt es Hinweise, dass sich psychische Symptome mit einer Hormontherapie manchmal vorteilhaft beeinflussen lassen. Zuverlässige Daten zu dieser Frage sind aber nicht vorhanden; die psychischen Symptome an sich stellen keine Indikation für eine Hormontherapie dar. Ob überhaupt eine medikamentöse Therapie notwendig ist, soll unabhängig von der Menopause beurteilt werden.
Osteoporose
Eine Hormontherapie hat nachgewiesenermassen eine günstige Wirkung auf die Knochendichte; in den WHI-Studien wurde zudem gezeigt, dass unter Hormonen auch die Frakturhäufigkeit reduziert ist. Dieser Effekt schwindet jedoch, wenn die Hormone abgesetzt werden. Da eine Osteoporose eine langfristige Behandlung erfordert, fällt eine Hormontherapie in der Regel ausser Betracht. Weitere therapeutische Entscheide bezüglich der Osteoporose sind unabhängig von der Menopause zu treffen. Ob eine Hormontherapie in Einzelfällen – bei einer Unverträglichkeit anderer Therapiemöglichkeiten – einmal längerfristig verabreicht werden soll, muss insbesondere gegen das erhöhte Schlaganfall- und Brustkrebs-Risiko abgewogen werden.
Schlussfolgerungen
Eine längerdauernde Hormontherapie nach der Menopause hat gesamthaft mehr Nachteile als Vorteile. Eine Minderheit der Frauen hat jedoch so ausgeprägte menopausale Beschwerden (insbesondere vasomotorische Symptome), dass eine zeitlich limitierte Hormontherapie indiziert sein kann. Nicht-hormonale Medikamente sind in diesen Fällen ungenügend wirksam.
Literatur
- 1) Pinkerton JAV. Menopause 2014; 21: 1298-1300
- 2) Leach MJ, Moore V. Cochrane Database Syst Rev 2012; 9: CD007244
- 3) Boardman HM et al. Cochrane Database Syst Rev 2015; 3: CD002229
- 4) Schierbeck L. Climacteric 2015; 18: 492-7
- 5) Smith NL et al. JAMA Intern Med 2014; 174: 25-31
- 6) Shufelt CL et al. Menopause 2014; 21: 260-6
- 7) Mohammed K et al. J Clin Endocrinol Metab 2015; 100: 4012-20
- 8) Chlebowski RT et al. JAMA 2010; 304: 1684-92
- 9) Marjoribanks J et al. Cochrane Database Syst Rev 2012; 8: CD004143
- 10) Beral V et al. J Natl Cancer Inst 2011; 103: 296-305
- 11) de Villiers TJ et al. Climacteric 2013; 16: 316-37
- 12) Manson JE et al. JAMA 2013; 310: 1353-68
- 13) Chlebowski RT, Col N. Lancet 2004; 363: 410-1
- 14) Holmberg L et al. Lancet 2004; 363: 453-5
- 15) Anderson GL et al. Lancet Oncol 2012; 13: 476-86
- 16) Beral V et al. Lancet 2015; 385: 1835-42
- 17) Racine A et al. CMAJ 2013: 185: 555-61
- 18) Liu B et al. BMJ 2008; 337: a386
- 19) Wallace RB et al. Am J Clin Nutr 2011; 94: 270-7
- 20) Bedell S et al. J Steroid Biochem Mol Biol 2014; 139: 225-36
- 21) Chiu HY et al. Menopause 2015; 22: 234-44
- 22) Norton S et al. Menopause 2014; 21: 574-8
Standpunkte und Meinungen
- Es gibt zu diesem Artikel keine Leserkommentare.
Copyright © 2024 Infomed-Verlags-AG
PK992
Verwandte Artikel
Gratisbuch bei einem Neuabo!
pharma-kritik abonnieren
-
Jahrgang 45 / 2023
Jahrgang 44 / 2022
Jahrgang 43 / 2021
Jahrgang 42 / 2020
Jahrgang 41 / 2019
Jahrgang 40 / 2018
Jahrgang 39 / 2017
Jahrgang 38 / 2016
Jahrgang 37 / 2015
Jahrgang 36 / 2014
Jahrgang 35 / 2013
Jahrgang 34 / 2012
Jahrgang 33 / 2011
Jahrgang 32 / 2010
Jahrgang 31 / 2009
Jahrgang 30 / 2008
Jahrgang 29 / 2007
Jahrgang 28 / 2006
Jahrgang 27 / 2005
Jahrgang 26 / 2004
Jahrgang 25 / 2003
Jahrgang 24 / 2002
Jahrgang 23 / 2001
Jahrgang 22 / 2000
Jahrgang 21 / 1999
Jahrgang 20 / 1998
Jahrgang 19 / 1997
Jahrgang 18 / 1996
Jahrgang 17 / 1995
Jahrgang 16 / 1994
Jahrgang 15 / 1993
Jahrgang 14 / 1992
Jahrgang 13 / 1991
Jahrgang 12 / 1990
Jahrgang 11 / 1989
Jahrgang 10 / 1988
Kennen Sie "100 wichtige Medikamente" schon?
Die Liste der 100 Medikamente sehen Sie auf der Startseite von 100 Medikamente.